29일 HLB(028300)와 제약바이오 업계에 따르면 지난해 11월 미국 식품의약국(FDA)은 리보세라닙-캄렐리주맙(중국 항서제약) 간암 치료제 허가를 위한 현장 실사를 완료했다. 그 결과 큰 문제없이 실사를 통과했다. 회사는 지난해 5월 FDA에 품목허가를 신청했고, 7월 본 심사 개시, 11월 현장 실사 등의 절차까지 완료했다. 이후 올해 3월 품목허가를 위한 최종 리뷰가 진행되고, 5월 최종 품목허가 여부가 결정되게 된다.
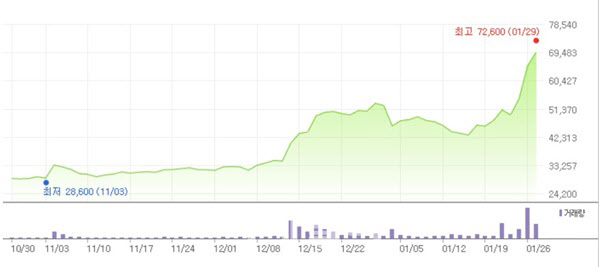
FDA 현장 실사에서 문제없이 통과됐다는 소식과 함께 허가 가능성이 높아졌다는 전망에 HLB 주가도 짧은 기간에 폭발적인 상승세다. 한국거래소에 따르면 HLB는 지난해 11월 1일 2만9100원이던 주가가 지난 1월 26일 6만5200원으로 약 4개월만에 124% 상승했다. 같은 기간 11월 1일 약 3조7541억원으로 코스닥 시가총액 6위던 HLB는 지난 26일 약 8조5038억원으로 약 127% 상승, 에코프로 형제 바로 뒤인 시가총액 순위 3위에 올랐다.
|
◇2027년까지 매출 3.1조-영업익 2.6조 목표
야후 파이낸스의 글로벌 간암 치료제 시장 리포트에 따르면 글로벌 간암 치료제 시장 규모는 2022년 약 24억 달러(약 3조2000억원)에서 연평균 18.6% 성장해 2030년 약 93억 달러(약 12조5000억원)에 달할 전망이다. HLB의 리보세라닙-킴렐리주맙 병용 치료제는 간암 1차 치료제 시장을 정조준 한다. 현재 관련 시장은 지난해 11월 말 기준 로슈 52%, 아스트라제네카 25%, 기타 23%로 분할하고 있다.
HLB 측은 리보세라닙-킴렐리주맙 FDA 허가시 폭발적인 성장을 확신하고 있다. HLB 관계자는 “리보세라닙-킴렐리주맙 간암 1차 치료제는 늦어도 5월 16일 이내 허가 여부가 결정될 것”이라며 “현재 간암 1차 치료제 시장은 로슈와 아스트라제네카 치료제 등이 출시됐지만, 여전히 새로운 옵션에 대한 니즈가 높다. 3년내 미국 등 글로벌 시장 점유율 약 50%, 매출 3조1000억원을 목표로 하고 있다”고 말했다.
특히 HLB는 영업적자도 빠르게 개선할 수 있을 것으로 내다보고 있다. 회사 관계자는 “올해 미국에서 리보세라닙이 신약으로 허가를 받을 가능성이 높은 만큼, 허가를 받게되면 현재까지의 영업적자는 큰 의미가 없을 것으로 보고 있다”며 “올해 하반기부터 리보세라닙과 캄렐리주맙을 통한 미국발 매출이 발생할 것이다. 해당 치료제의 영업이익률이 높은 만큼 빠른 시간안에 실적 턴어라운드가 가능할 것”이라고 강조했다.
HLB 자신감 배경, 데이터-영업이익률 85%
HLB의 자신감에는 경쟁약 대비 우수한 효능과 높은 영업이익률이 그 배경으로 자리잡고 있다. 현재까지 간암 1차 치료제로 로슈 아테졸리주맙-베바시주맙 병용, 아스트라제네카 더발루맙-트레멜리무맙 병용, 에자이 렌바티닙, 바이엘 소라페닙이 허가받았다. 이 중 생존 기간(OS) 수치는 로슈 19.2개월, 아스트라제네카 16.4개월, 에자이 13.6개월, 바이엘 10.7개월이다.
특히 주목할 것은 OS 데이터가 더 낮은 아스트라제네카 치료제가 시장을 선점했던 로슈 치료제 를 빠르게 잠식하고 있는데, 이는 로슈 치료제의 부작용 이슈가 크게 작용했다는 분석이다. HLB 관계자는 “아스트라제네카 치료제가 효과성 측면에서 로슈 치료제 대비 이점이 없지만, 시장 점유율이 빠르게 확대되고 있는 것은 아테졸리주맙과 베바시주맙 병용 치료제의 부작용 때문”이라며 “로슈 치료제 복용 환자 77%가 12개월 이내 치료를 중단했고, 평균 치료 중단 기간은 5.1개월에 달한다. 이는 위장간 출혈로 인한 복용 중단 및 간기능 악화된 환자에게 악효가 없어 다른 약을 대체됐을 확률이 큰 것으로 판단된다”고 말했다.
반면 리보세라닙-캄렐리주맙 병용 치료제는 간암 1차 치료제 중 역대 최장 생존기간인 22.1개월을 나타냈다. 로슈 치료제처럼 중대한 부작용도 나타나지 않았다는 게 회사 측 설명이다. 또 로슈 치료제는 간기능 저하 능력을 나타내는 지표인 ALBI 기준 1등급 환자에게만 약효를 나타냈지만, HLB 치료제는 ALBI 1등급 환자는 물론 2등급 환자에서도 효과가 나타났다.
회사 측은 리보세라닙이 높은 영업이익률로 실적 반등에도 기여할 것으로 내다보고 있다. HLB 관계자는 “리보세라닙이 바이오 의약품이 아닌 합성의약품이고, 중국에서 대량 생산을 해서 원가율은 극히 낮은 수준이다. 판매를 위한 판관비 등을 고려하면 리보세라닙 영업이익률은 약 85%로 추산하고 있다”며 “리보세라닙 허가를 대비해 이미 유통 판매 계획도 다 수립한 상태다. 올해 9월 정도부터 판매를 시작하는 것을 목표로 하고 있다. 치료제 가격도 기존 치료제들보다 경쟁력을 가질 것으로 보고 초기 시장 진입 시간을 거쳐 본격적으로 시장 점유율을 확대할 수 있을 것으로 내다보고 있다”고 말했다.