|
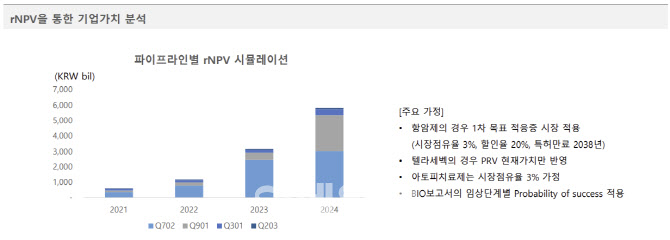
큐리언트가 자사의 시총이 저평가됐다고 판단하는 근거는 보유 중인 항암제 파이프라인의 가치다. 큐리언트는 거래 정지 기간에 항암제 임상 단계가 진전되면서 파이프라인별 위험조정순현재가치(rNPV)가 급상승했다는 게 회사 측의 판단이다.
|
특히 Q702와 Q901는 모두 미국 머크(MSD)와 면역관문억제제 ‘키트루다’ 병용임상을 위한 공동개발 계약을 체결한 물질이다. 국내에서 2가지 신약후보물질로 키트루다 병용임상을 진행하는 곳은 큐리언트가 유일하다. 큐리언트는 머크와 공동 임상개발팀도 구성했으며, 키트루다를 무상 공급 받게 된다.
Q702은 ‘Axl’ ‘Mer’ ‘CSF1R’ 세 가지 수용체를 동시에 저해하는 삼중저해 면역항암제다. 면역세포와 암세포에 동시 작용한다는 게 특징이다. 큐리언트 관계자는 “Q702는 기존 면역항암제를 처방 후 재발되거나 현재 치료법이 없는 환자들을 대상으로 하기 때문에 키트루다 병용 투여를 할 경우 면역 조절을 통한 항암 치료 효과가 더 커질 것”이라고 기대했다.
반면 Q901은 암세포의 DNA 복구억제를 통한 유전체 불안정성을 높이는 기전을 갖고 있다. 키트루다는 유전체 불안전성이 낮은 암종에는 약효가 잘 발휘되지 않는 경향이 있다. 이 때문에 Q901과 키트루다를 병용하면 기존에 키트루다만으로는 치료가 되지 않던 암종도 치료 가능해질 것으로 기대된다.
큐리언트 관계자는 “Q702 병용임상을 진행 중이었던 머크가 Q901 병용 임상을 먼저 제의했다”며 “완전히 다른 기전 2개의 신약을 대상으로 병용요법 시도를 하게 된 것”이라고 언급했다.
큐리언트는 오는 4분기부터 Q702 병용요법 임상 1b/2상 환자 투약을 시작할 예정이다. 해당 임상은 미국과 한국에서 약 142명의 진행형 고형암 환자를 대상으로 진행된다. Q702 단독요법인 미국 임상 1/2상도 순항 중이다. 해당 임상은 2020년 4월에 개시했으며, 내년 11월에 완료될 전망이다.
Q901도 4분기부터 미국에서 단독투여 임상 1/2상의 환자 투약을 시작할 예정이다. 큐리언트는 진행형 고형암 환자 70명을 대상으로 해당 치료제의 안전성, 최대내약용량, 용량제한독성 등을 확인하고 임상 2상 용량을 결정할 계획이다. Q901의 키트루다 병용 임상은 내년 4분기에 개시될 것으로 예상된다.
큐리언트 관계자는 “큐리언트는 거래정지 이전과 비교해 항암제 파이프라인의 개발 단계가 진전되면서 rNPV가 급격히 상승했다”며 “거래정지 기간 중 주식시장의 조정 폭을 감안하더라도 시장에서의 재평가를 기대한다”고 말했다. 이어 “항암 파이프라인 개발이 잘 진척되면서 내부적으로는 상당히 고무된 분위기”라고 덧붙였다.







![한 놈만 아득바득 이 갈던 명재완에...별이 졌다 [그해 오늘]](https://image.edaily.co.kr/images/vision/files/NP/S/2026/02/PS26021000001t.jpg)

