16일 제약·바이오업계에 따르면 희귀소아질환에 대한 PRV 프로그램 연장 법안이 미국 상원을 통과하는 데 실패했다. 이로써 PRV 발급분야는 열대소외질환으로 축소됐다.
PRV는 1년 이상 걸리는 신약승인 검토 기간을 6개월로 줄일 수 있는 권리로, 제약사들로 하여금 희귀질환 및 중저 소득국에서 발병률이 높은 질병의 치료제 개발을 독려하기 위해 FDA가 제공하는 인센티브 제도다. 일종의 바우처인 PRV를 수령한 회사는 제3자에 자유롭게 매매할 수 있다. 기존 △열대소외질환 △희귀소아질환 △공중보건 위기대응과 관련된 치료제 개발시 PRV가 발급됐다.
앞서 지난 2023년 10월 공중보건 위기대응 의약품에 대한 PRV 일몰이 먼저 이뤄졌고 마지막까지 연장 여부를 두고 미국에서 논란이 뜨겁던 희귀소아질환에 대한 PRV 발급 프로그램도 연장없이 일몰이 결정된 것이다. 이번 일몰로 지난해 12월 20일까지 희귀소아질환의약품으로 지정(RPDD·Rare Pediatric Disease Designation)됐던 신약후보물질에 한해 내년 9월까지 임상 2상 조건부 허가를 받으면 PRV를 발급받을 수 있다.
특히 희귀소아질환은 가장 PRV 발급건수가 많은 분야였기에 의미하는 바가 크다. 전체 PRV 발급건수 중 희귀소아질환으로 인한 발급이 차지하는 비중은 75%에 달했다. 이 때문에 희귀소아질환 PRV 발급 프로그램이 종료되면 시장에 유통되는 PRV 자체의 개수가 줄어들 수밖에 없어 결과적으로 PRV의 가치가 높아질 것으로 예상된다. PRV 거래가격은 수요와 공급에 의해 변동되는데 PRV 발급량이 가장 많았던 때는 6700만 달러(약 977억원) 수준에서 거래될 때도 있었고, 발급량이 적을 때는 3억5000만 달러(약 5100억원)에서 거래되기도 했다.
|
연구·개발 자금이 넉넉지 않은 국내 바이오벤처 중에서도 PRV를 거래해 이를 자금으로 활용하려던 곳이 많았다. 이 때문에 PRV 프로그램 일몰 여부는 국내에서도 관심이 큰 이슈다.
지난 2023년 1월 GC녹십자(006280)는 노벨파마와 공동개발 중인 산필리포증후군 A형 치료제 후보물질 GC1130A로 RPDD 지위를 확보했다. 피알지에스앤텍(PRG S&T)도 지난 2020년 1월 소아조로증 치료제 후보물질 프로제리닌(PROGERININ)에 대해 RPDD 지위를 획득했다. 2023년 12월에는 줄기세포치료제 전문 바이오벤처 메디노가 신생아 저산소성 허혈성 뇌병증(HIE) 치료제로 개발 중인 ‘히스템’(HIEstem)이 RPDD를 받았다.
다만 개발속도를 감안했을 때 이들 회사의 PRV 수령 가능성은 높지 않아 보인다. GC녹십자와 노벨파마가 개발 중인 GC1130A은 지난해 1상 임상시험계획(IND)을 승인받아 패스트트랙으로 지정되기도 했지만 임상 1상 종료 시점이 오는 2027년 6월로 예정돼 있다.
피알지에스앤텍 역시 지난 2023년 8월 FDA로부터 프로제리닌의 임상 2상 승인을 받았는데 미국국립보건원(NIH)이 운영하는 임상정보 웹페이지 클리니컬 트라이얼에 따르면 올해 임상 2상을 개시해 오는 2027년 1월 종료하는 것으로 돼 있다. 메디노의 히스템도 아직 임상 1상 단계에 있다. 이밖에 닥터노아바이오텍도 지난해 뒤센근이영양증(DMD) 치료제 후보물질 NDC-026이 RPDD를 받았지만 해당 물질은 아직 전임상 단계에 있어 PRV 수령 대상에서 벗어나 있는 상태다.
이 때문에 임상 일정이 앞당겨지지 않는 한 국내 기업들의 희귀소아질환 분야 PRV 수령은 사실상 어려울 것으로 예상된다.
|
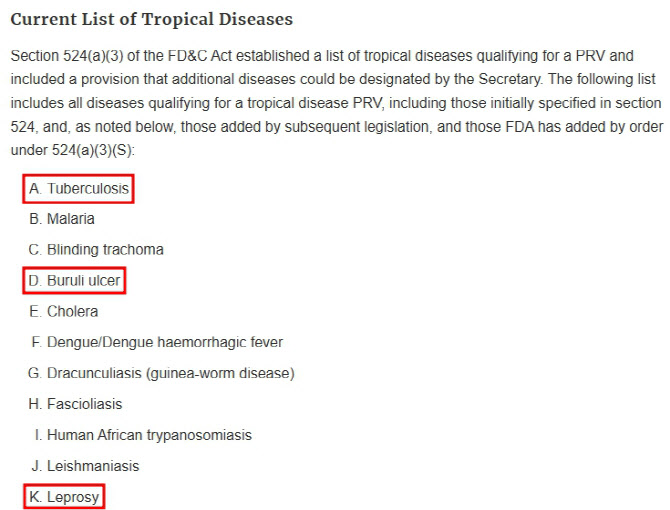
일몰 이슈가 없는 열대소외질환에서 PRV 수령을 노리는 곳도 있다. 큐리언트(115180)와 리가켐바이오(141080)다. 리가켐바이오는 항생제 ‘델파졸리드’를 다제내성 결핵 치료제로 개발 중인데 결핵은 대표적인 열대소외질환 중 하나다. 현재 델파졸리드는 미국 FDA로부터 희귀의약품으로 지정돼 임상 2상을 진행 중이다.
큐리언트는 아프리카, 호주, 남미 등에서 주로 발생하는 부룰리궤양 치료제 ‘텔라세벡’(Q203)으로 PRV 수령을 기대하고 있다. 텔라세벡은 지난 2023년 국제 결핵치료제 개발기구인 TB얼라이언스에 기술수출됐는데, 당시 선급금 및 마일스톤을 받는 대신 PRV 권리와 상업화 이후 로열티를 수령하도록 계약이 이뤄졌다.
텔라세벡은 최근 40명을 대상으로 한 임상 2상 환자 투약을 마쳤다. TB얼라이언스는 200명을 대상으로 한 확장임상을 통해 임상 2상을 최종 종료하고 조건부 허가를 추진할 예정인데 이때 PRV 수령 여부가 결정될 전망이다. 회사는 PRV 수령 및 조건부 허가 여부가 결정되는 시점을 내년으로 내다보고 있다.
Q203은 부룰리궤양 치료제 외 한센병 및 결핵 치료제로도 개발 중이기에 부룰리궤양 치료제로 허가를 받지 못할 경우 다른 질환을 타깃으로 한 후속 임상에서 PRV를 노려볼 수도 있다. 다만 PRV는 한 물질당 한 번만 수령할 수 있어 세 가지 적응증 치료제로 모두 허가를 받더라도 중복 수령은 불가능하다.
큐리언트 관계자는 “최근 PRV 딜들은 1억5000만 달러(약 2200억원) 선에서 이뤄지고 있다. PRV 공급 감소로 앞으로 지속해서 가격이 오를 것으로 보이는데 오는 2026년에는 3000억원 이상의 가치를 가질 것으로 예상된다”며 “회사가 PRV를 수령하게 된다면 그때의 현금흐름을 감안해 매매 여부 및 매매 시점을 결정할 것”이라고 말했다.


.png)
.png)










!['280만원 전망' 아이폰 폴더블, 핵심 기능 5가지 빠지나[모닝폰]](https://image.edaily.co.kr/images/vision/files/NP/S/2026/04/PS26042700108t.jpg)